構造による作用
現代医学において、ヒトの疾患に関する最初のクルクミンの研究は、1937年にOppenheimerによって報告されました。それ以降、クルクミンは、抗酸化物質から抗炎症物質、抗癌物質まで、幅広い生物学的活性に関する4,000以上の報告がなされています。多岐にわたるこれらの効果は、分子が相互作用して複数の標的を調節する能力によるものであるとされています。
いくつかの分子標的と相互作用する能力を有するクルクミンは、従来の「1つの化合物―標的」の概念ではなく、「1つの化合物―複数の標的」という概念であり「polypharmacology(ポリ薬理学)」という用語で表されます。
クルクミンは、標的に直接的・間接的結合し、調節(アップレギュレーションまたはダウンレギュレーション)することによりその生物学的活性を示します。これらの生物学的活性は、メチレン架橋によって連結された2つのフェニル基の化学構造による影響と考えられます。このような柔軟な化学構造は、いくつかの生化学的経路を調節または干渉するため、クルクミンに多様性をもたらします。
クルクミンの標的には、炎症因子、酵素、成長因子、転写因子、キナーゼ、受容体および金属イオンが含まれます。
生物学的活性と化学構造の分析
前述のように、クルクミンは間接的・直接的に二重結合および非二重結合に作用するので、酵素、キャリアタンパク質および核酸をはじめとする多くのタンパク質分子(例えば腫瘍壊死因子-α、シクロオキシゲナーゼ-1および2)に対する分子モデリングおよびドッキング研究がなされてきました。
クルクミンおよびそのアンマージンボトムは非常に低濃度でこれらのタンパク質と結合します(結合定数はnM-μMの範囲で検出されています)。
その独特な構造により(いくつかの異なる立体配座を示すことができます)、親和性が高くタンパク質に直接結合します。フェニル、ヒドロキシル、メトキシルおよび1,3-ジカルボニル官能基部は、静電相互作用を持ち強い結合力が増します。
さらにクルクミンは、β-ジケトン部分のケト-エノールの異性体を持ちます。安定しているエノール体は、分子の中間部分が水素結合供与体および受容体の両方として作用することが可能であり、標的タンパク質の活性部位に存在する正電荷の金属のキレート化剤としても作用します。
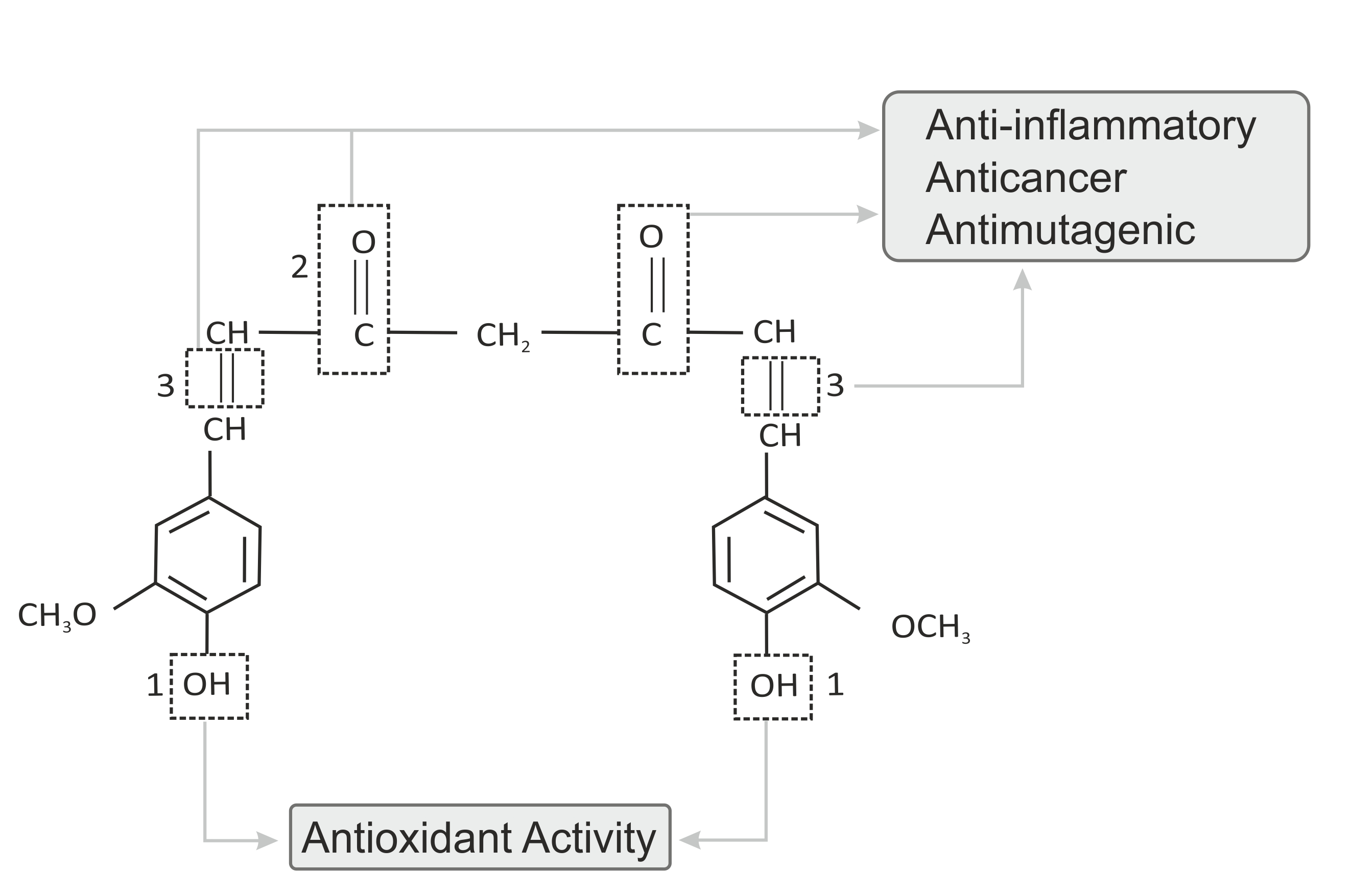
引用論文: Majeed M. and Badmaev V. Curcuminoids-Pharmacological Actions Including Pre-Clinical and Clinical Evaluations. In: Curcuminoids: Antioxidant phytonutrients, New Jersey, Nutriscience Publishers Inc., 2003;pp. 32.
